Pfizer e Johnson & Johnson dão primeiro passo para que vacinas sejam autorizadas no Brasil
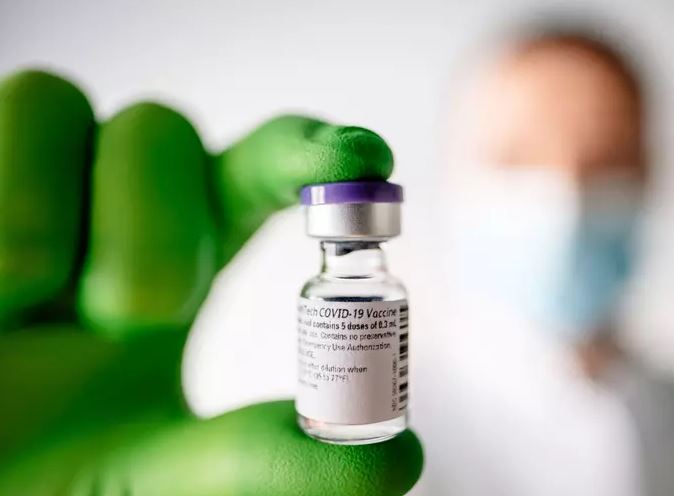
Foto: BioNTech/Divulgação via Reuters
As farmacêuticas Pfizer e Janssen (da Johnson e Johnson) solicitaram à Agência Nacional de Vigilância Sanitária (Anvisa) um certificado de boas práticas pela fabricação das vacinas. Essa é uma das etapas que antecedem o pedido de registro e de liberação dos imunizantes para usos emergenciais no Brasil.
AstraZeneca, que fabrica a vacina em parceria com a Oxford, e a Sinovac, que tem acordo com o governo de São Paulo, já solicitaram esse certificado também e passaram por inspeções, ainda sem resposta. As equipes da Anvisa que foram pessoalmente até os laboratórios já retornaram ao Brasil. Eles ficarão de quarentena por 14 dias, sob trabalho remoto. Em nota, a Anvisa afirma que aguarda informações complementares das fabricantes antes de conceder o certificado.
“A etapa finalizada é essencial para que as vacinas a serem disponibilizadas no Brasil tenham qualidade e segurança. Todos os esforços estão sendo adotados para que as certificações sejam concluídas com a maior brevidade possível”, explica a agência.
Até agora, nenhuma fabricante solicitou a liberação em caráter emergencial ou o registro definitivo das vacinas no Brasil.
No sábado (12), o governo entregou ao Supremo Tribunal Federal um Plano Nacional de Imunização.
“A distribuição cronológica no decorrer dos meses, inicialmente organizada, alterna semanalmente as vacinas de rotina e as vacinas destinadas aos grupos prioritários específicos das campanhas da vacina covid-19 e influenza, e observa os cronogramas previstos já apresentados pela AstraZeneca”, diz o documento.
O plano não traz, no entanto, a data de início da vacinação no Brasil. De acordo com o documento, para “a incorporação da nova vacina no Calendário Nacional de Vacinação faz-se necessária a aprovação da vacina pela Agência Nacional de Vigilância Sanitária (Anvisa)”.
CNN Brasil